| 送交者: 苦难与荣耀[☆★★声望品衔12★★☆] 于 2020-06-11 0:47 已读 1592 次 2 赞 | 苦难与荣耀的个人频道 |
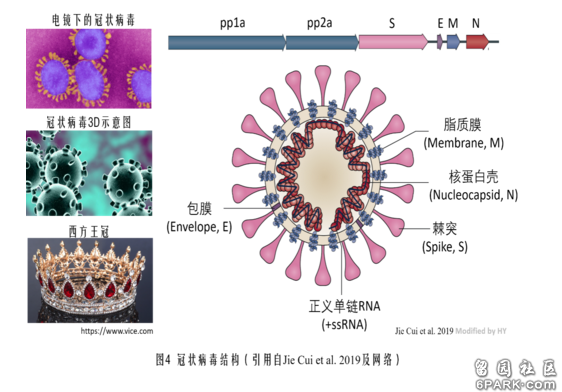
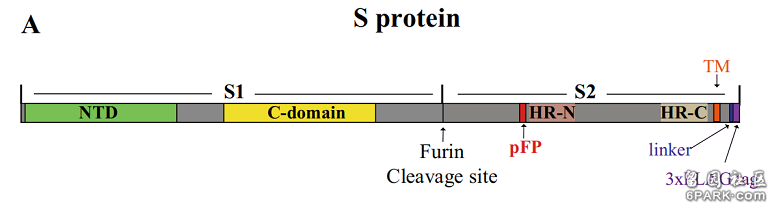
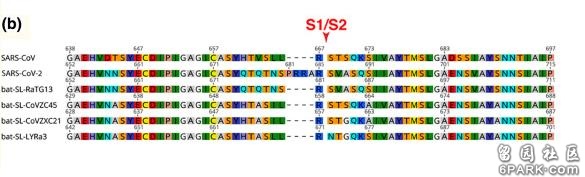
昨天,在本版发了一篇回应帖“对版神再度评论帖的答复” https://club.6parkbbs.com/life2/index.php?app=forum&act=threadview&tid=15471389 6park.com帖子发出,人潮人海的生活百态众网友不约而同,纷纷礼让七分,绕道而行,让人受宠若惊。 6park.com刚才上来,总算在帖子下捡到块砖头,上面赫然写着“苦难与荣耀的文章只不过是非专业人士的牵强附会” https://club.6parkbbs.com/life2/index.php?app=forum&act=threadview&tid=15472020 6park.com感谢hulizhi网友赐砖!一个帖子下面,连块砖头都没有,那能叫帖子?那是官家的告示,或者商家的广告。 6park.com“灵感源自碰撞”,“真知出于辩论”。发帖,就要敢于直面无情的砖头,真相,离不开砸出的鲜血。意见交锋可喜,遭逢唯恐无沙埋头的鸵鸟可悲。“hulizhi”网友的果敢、自信、爱憎分明令人肃然起敬,得他授予“非专业人士”称号,深感荣幸,我的头衔又多了一个,可喜可贺。 6park.com转入正题。在应答“hulizhi”网友的评论内容之前,有必要先做一些简要说明,以便各位网友了解相关背景。 6park.com下图右侧,示意了冠状病毒的蛋白序列结构,及病毒体构造。 6park.com6park.com图中冠状病毒外部的红色突起,叫做S蛋白,或Spike蛋白,刺突蛋白,棘突蛋白。S蛋白是冠状病毒与宿主细胞受体结合,进而感染宿主细胞的钥匙。 6park.comS蛋白由两部分组成,一部分是S1蛋白,位于S蛋白的外部,另一部分是S2蛋白,位于S蛋白的下部,和病毒的包膜连在一起。如果把S蛋白看成是打开宿主细胞(如人体细胞)的钥匙,那么,S1蛋白相当于钥匙的“钥齿”部分,S2蛋白则相当于钥柄部分。 6park.com关于SARS-CoV-2(新冠)病毒的来源,有两种观点,一种认为它是自然变异产生的,另一种则认为它是在实验室人工干预下产生的。 6park.com如果SARS-CoV-2是自然变异产生的,那么,它是由哪种病毒演化而来的呢?研究发现,与SARS-CoV-2存在时间进化关系的已知病毒中,亲缘关系最近的,是一种叫做CoVZC45的类SARS冠状病毒。这一病毒提取自2017年从舟山捕获的蝙蝠,所以通常也称作舟山蝙蝠病毒,它的全基因组序列已于2018年上传至国际基因库全球共享。舟山蝙蝠病毒其实有两株,另一株是2015年得到的CoVZXC21,它与SARS-CoV-2相似度87.3。 6park.com一方面,CoVZC45与SARS-CoV-2基因相似度为87.5,另一方面,二者也有多处明显区别,其中的两个是: a) CoVZC45的S1蛋白不能与人体细胞受体ACE2(血管紧张素转换酶II)结合,从而无法感染人。众所周知,SARS-CoV-2则有强大的人际感染、传播能力。 b) CoVZC45没有酶切位点,而SARS-CoV-2则有酶切位点。 6park.comSARS-CoV-2的酶切位点恰恰位于S蛋白的两个亚基S1蛋白、S2蛋白的交界处,见下图。这个位置的酶切位点给SARS-CoV-2带来了不只一个极为强悍,极为可怕的功能。 6park.com 6park.comCoVZC45没有酶切位点,但只要在CoVZC45蛋白序列的S1、S2交界处,插入四个氨基酸(残基,对应4*3=12个碱基对)“PRRA”,其中的“RRA”,与原序列中紧邻的“R”,就构成了SARS-CoV-2的furin酶切位点“RRAR”。参见下图,图中第二行是SARS-CoV-2的氨基酸序列(或叫蛋白序列),第四行是CoVZC45的氨基酸序列。 6park.com 6park.com下面这个图可以看得更清楚一些。 6park.com 6park.com现在,各位网友对基本情况应该已有所了解,下面,我开始答复hulizhu网友的评论。加黑内容来自评论。 6park.com首先,请问hulizhu网友,既然您火眼金睛,看出我是“非专业人士”,那么,比我专业的您,应该知道下述问题的答案:酶切位点是什么?含几个碱基对?几个氨基酸?长度长不长?是大片断还是小片断? 6park.com这些问题,在下述的讨论中将要涉及到,它们的答案,在我前面的交待中其实已经讲到了。 6park.com“大片段变异(如基因重组等)绝非可以忽略的误差!” 6park.com请问,“大片断变异”怎么把大片断序列塞到S1/S2位置上产生小片断的酶切位点?能否描述一下可能的实现过程?难道先用大片断序列把CoVZC45的S蛋白吃撑,再拉出一大部分,恰好剩下了那一小截?这种情况机率有多大?忽略它造成的估算偏差能有多大? 6park.com“事实上,病毒不仅可以通过基因重组获得突变,甚至可以从宿主基因组中获取基因片段!” 6park.comCoVZC45可在哪些情况下,与哪些生物通过基因重组获得酶切位点突变?它可以从哪些宿主的基因组中获取酶切位点片断?这两种途径的可能性有多大?如果可能性很大,为何CoVZC45所在的β谱系的冠状病毒,绝大多数都未能获得酶切位点?这几个问题您的答案是什么? 6park.com“恰恰相反,自然界中各生物体的基因组序列差异不可能‘大致均匀分布’。” 6park.com您的这个说法跑题了,应修正为“恰恰相反,自然进化情况下,祖先(CoVZC45)与后代(SARS-CoV-2)之间基因序列上的差异不可能‘大致均匀地分布’”。 6park.com因为,您是在辩驳我的观点,我的原话是“自然进化情况下,祖先(CoVZC45)与后代(SARS-CoV-2)之间基因序列上的差异应该大致均匀地分布”。 6park.com或者说,我们讨论的是,‘自然进化情况下祖先与后代之间的基因序列差异’,而非“自然界中各生物体的基因组序列差异”,这是两个天差地远的问题。讨论应该针对彼此的观点有的放矢,不该转移话题,但我相信您是无心之失,不是有意移花接木,偷梁换柱。 6park.com“b. 自然进化情况下,祖先(CoVZC45)与后代(SARS-CoV-2)之间基因序列上的差异应该大致均匀地分布,相对协调地产生,不应该出现仅某个部分大量变异,而其余部分都高度稳定的情况。其他所有蛋白的一致性都>=94%,唯独S1蛋白的一致性仅为69%,如此突兀的“自然变异”,在自然界很难找到先例。 ” 恰恰相反,自然界中各生物体的基因组序列差异不可能“大致均匀分布” 6park.com上面最后一句是您的评论(前面刚刚提到过了),之前b.之后的内容来自我的“实验室合成、编辑SARS-CoV-2简明教程”一文。 https://club.6parkbbs.com/other/index.php?app=forum&act=threadview&tid=12996959 6park.com如果您反对我所说的 “不应该出现仅某个部分大量变异,而其余部分都高度稳定的情况。其他所有蛋白的一致性都>=94%,唯独S1蛋白的一致性仅为69%,如此突兀的“自然变异”,在自然界很难找到先例。” 6park.com这一说法,那么,您是否能举出三个情况相似的进化例子?您即便只能举出一个例子,我也认可。 6park.com同时,我还希望您解释一下,CoVZC45(祖先)与SARS-CoV-2(后代)的各蛋白中,为何独独S1蛋白发生了那么大面积的变异?什么样的自然环境或自然情况,能促成这么不均衡的变异? 6park.com“楼主明显不知道在生物体基因组中存在高保守区域(highly conservative region)。在这些区域中突变很少发生。而在另一些区域,如流感病毒的H和N基因位置的突变率则会非常高。” 6park.com我有点困惑了,您是学东西一瓶子不满,半瓶子晃荡,不懂装懂?还是瞒天过海,故意含混糊弄人? 6park.com“其他所有蛋白的一致性都>=94%,唯独S1蛋白的一致性仅为69%”这个事实,您居然能用高度保守序列来解释?真是服了You。高度保守序列在全部基因组序列中所占的比例可能有这么大吗?!除了S1蛋白,舟山蝙蝠病毒CoVZC45其它所有蛋白序列都大比例变成高度保守序列了?您这个重大发现,发表了吗? 6park.com 6park.com“专业”与否,是看印制的名骗,还是看所做的事情? 6park.com开个玩笑,hulizhu网友,您的专业名片掉色了,重印十盒新的吧。 6park.com 6park.com 6park.com贴主:苦难与荣耀于2020_06_11 0:49:44编辑 6park.com贴主:苦难与荣耀于2020_06_11 1:10:41编辑 6park.com贴主:苦难与荣耀于2020_06_11 2:11:01编辑 6park.com贴主:苦难与荣耀于2020_06_11 2:34:12编辑 6park.com贴主:苦难与荣耀于2020_06_11 6:38:34编辑
贴主:苦难与荣耀于2020_06_11 7:05:16编辑