| 送交者: 索探[★★★网络贵族★★★] 于 2016-12-03 8:56 已读 2129 次 4 赞 | 索探的个人频道 |
北京大学的研究者开发出一种新型疫苗研发技术,通过在天然病毒株遗传序列中引入过早终止密码子,使得改造后的病毒在普通细胞中丧失复制增殖能力,但却保留完全的感染活性。研究者利用这种完全活性的病毒制作疫苗,能够有效诱发强大的体液、粘膜以及免疫T细胞介导免疫反应应对抗原性病毒,甚至能中和已受感染者体内存在的病毒株。这种疫苗技术有望成为一种应对几乎所有病毒的普适性方法,特别是全球众多致命性病毒。
该研究结果发表于12月2日《Science》上,并被称为疫苗研发领域的“革命性突破”。
这项研究打破了传统疫苗研发的两项禁忌:一项是利用活体的、完全感染性的病毒作为疫苗,第二项是将该疫苗注射进感染同种病毒的将死动物体内。根据论文结果,接受该疫苗的受感染动物最终都治愈了。
这项突破能够大幅简化疫苗生产流程、提高研发效率,有望使科学家在病毒爆发数周内迅速研发出针对多种病毒(如禽流感、埃博拉、艾滋病等病毒)的有效疫苗、甚至能够彻底治愈。
研究者在疫苗活体病毒的遗传密码中引入过早终止密码子(PTC),从而使得该病毒的自我扩增机制失效,同时完全保留其感染性以激活宿主动物细胞的免疫反应。
同时,研究者利用遗传密码扩增(Expanded genetic code)技术,使得在普通细胞中不能增殖的病毒疫苗能够在一种转基因细胞系中实现增殖和批量化生产。
通常,医用保留完全感染性的活体病毒作为疫苗是传统疫苗研发的一大禁忌,因为病毒的增殖速度十分惊人。当前市场上广泛售卖和使用的疫苗都是灭活或者较弱感染性的病毒。
通常,批准临床使用的疫苗都会通过改造病毒结构降低其感染性,但同时也降低疫苗的有效性。此外,目前对于全球多种致命性病毒甚至还未研发出任何有效的疫苗。
项目负责人——北京大学药学院教授周德敏
周德民教授在《南华早报》的采访中表示:“长久以来,在对抗病毒的战争中人类一直处于下风。现在,我们终于有了新的武器,几乎可以应对所有的病毒及其突变体,这将逆转战争的局势。”
周德民团队利用活体禽流感病毒制作疫苗,并进行了包括小鼠、荷兰猪和白鼬在内的疫苗注射动物实验。虽然病毒入侵宿主后对宿主细胞产生了严重损伤,但这些活性病毒自身并未发生复制增殖。随后,宿主免疫系统启动,逐个清除细胞内的病毒。仅在注射疫苗三天后,宿主体内的病毒已被完全清除,同时获得了对抗该病毒的免疫能力。
然后,研究者又向感染禽流感病毒的小鼠注射疫苗,最终小鼠迅速获得康复。
研究表明:在宿主体内,这种人工改造的活性病毒与野生型病毒发生遗传重组,所以重组后的病毒也丧失自身复制能力。
周德民表示:“这不仅是疫苗,也是一种药物。”
该研究所用改造型活性禽流感病毒与其天然型病毒株有99%的相似性。研究只是随机选取了编码病毒核蛋白的遗传序列上的一个密码子*,并通过定点突变将其替换为终止密码子,最终制造出同时保留感染活性而丧失增殖能力的“过早终止密码子”(PTC)病毒株。
*密码子(codon)是指信使RNA上的一个核苷酸三联体序列,在蛋白质翻译合成时代表某一种氨基酸。终止密码子(terminationcodon)是代表翻译终止的核苷酸三联体序列。
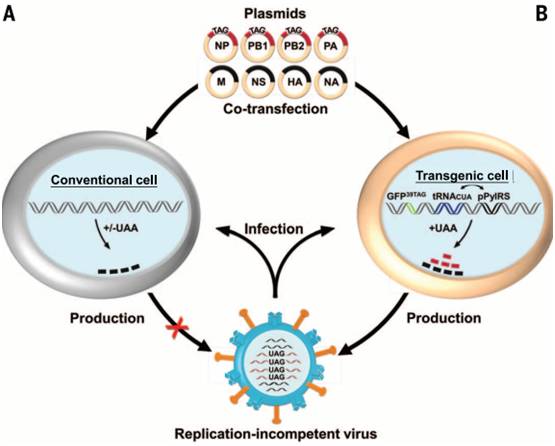
人工改造后丧失增值能力的活性病毒。左路:该病毒感染普通细胞无法实现自我增殖;右路:该病毒感染特殊转基因细胞,实现自我扩增和批量化疫苗生产。
通常,病毒需要宿主体内多种氨基酸来合成其蛋白质外壳,而改造后的病毒只能利用一种特殊的人工合成氨基酸合成外壳进行复制。宿主体内缺乏特殊的氨基酸,所以病毒无法复制增殖,最终只能“饿死”。
研究者基于一种人工转基因细胞系进行疫苗病毒的扩增和批量生产,这种转基因细胞系含有这种特殊的氨基酸作为病毒扩增原料。
据周教授称,这种疫苗技术前景很好,可能很快就会投入使用。比如,一旦有了像非典病毒这种大爆发时,这种疫苗技术可以帮助国家快速响应并控制病情。
对于任何病毒爆发,研究者可以快速从感染者体内分离得到这种未知病毒株,并只需选取病毒遗传序列的一个密码子并改造为终止密码子病毒株,新病毒就可以作为疫苗推广接种。
所有这一系列的研发过程可以在短短几周内完成,达到快速响应、及时控制病情。这种疫苗同样也可以用于治疗已经感染病毒的病人。
周教授表示,“这种方法的副作用很小,受试者几乎感觉不到任何副作用。我认为,这种技术很快就会造福人类。”
研究团队已经为此技术申请了专利,同时他们正在联系疫苗厂家以尽快开展临床试验。
传统的疫苗研发流程复杂而漫长,研究者需要弄清病毒的结构和行为之后,才能对症下药。但是这种新方法大大简化了疫苗研发的流程,我们只需要改造病毒遗传序列的几个碱基就可以生产疫苗。同时,因为这些编码密码子的三联碱基序列存在于几乎所有的病毒内,所以这种方法有很强的普适性。
中科院病原微生物与免疫国家重点实验室研究人员孟颂东表示,周教授团队的研究是一种“全新的、前所未有的方法”,为我们对抗病毒指明了新路。
然而,他同时也表示了对这项研究近期用于临床的担忧。这种人工改造的病毒有可能发生意外的突变,打破原本对其自我复制性的限制,这将带来不可估量的后果。此外,人造病毒和天然病毒重组后的结果可能并不像我们预期那样好。
孟松东表示:“这项研究的风险在于改造后的病毒可能变得毒性更强,甚至复制更快。我认为,没有任何国家的卫生部门,尤其是中国,会批准在病人体内接种活性病毒疫苗。”
参考:http://science.sciencemag.org/content/354/6316/1170?utm_campaign=toc_sci-mag_2016-12-01&et_rid=171304363&et_cid=1031518